生命的尽头是AI?谷歌发布AlphaFold 3 ,可预测所有蛋白质、DNA、RNA及交互
近日,谷歌DeepMind携手制药行业的创新力量Isomorphic Labs,共同推出了全新的人工智能模型——AlphaFold3。这一里程碑式的升级不仅突破了蛋白质结构预测的局限,更将预测能力扩展至DNA、RNA、配体等生命分子的三维结构及它们之间的相互作用,预示着人工智能在细胞生物学领域的新纪元。

AlphaFold 3的核心在于其独特的Evoformer深度学习架构和庞大的生命分子训练数据集。该模型首先处理输入的分子数据,随后通过一种类似图像生成器的扩散网络,从原子云出发,历经多次迭代优化,最终生成高精度的分子结构预测。令人瞩目的是,AlphaFold3在无需任何结构信息输入的情况下,其预测准确度相较于现有方法提升了高达50%,对于某些相互作用类别,准确度甚至翻倍。
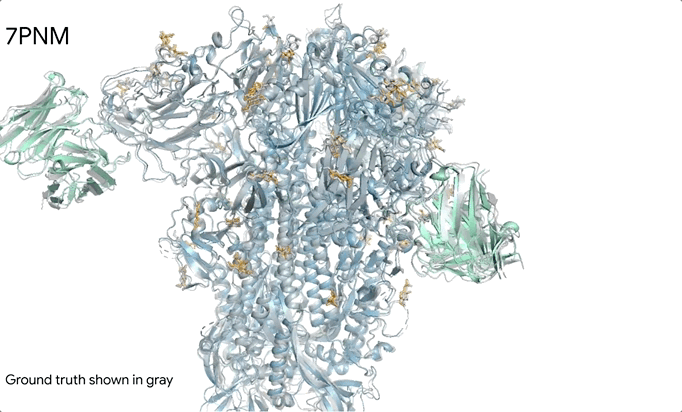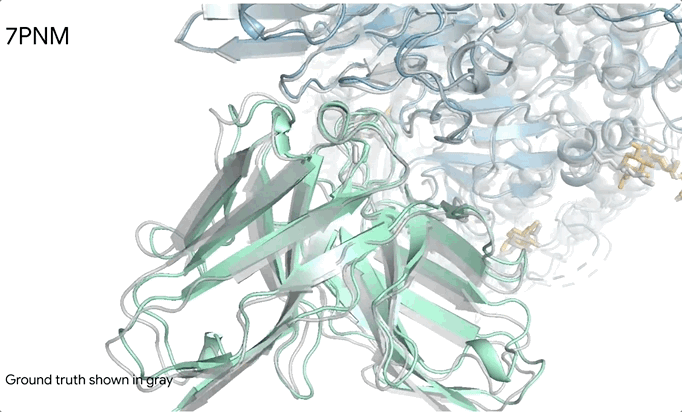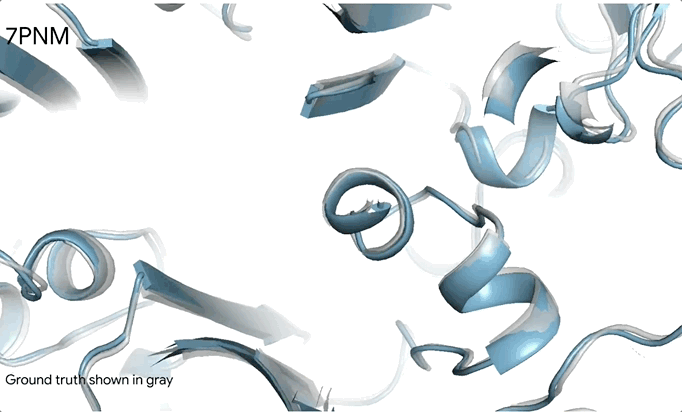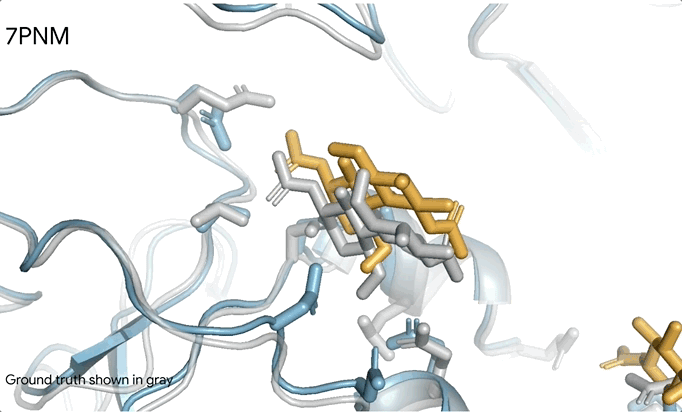
这一革命性的突破使AlphaFold3成为首个超越传统基于真实生物分子结构预测工具的AI系统。更令人惊叹的是,即便在训练数据极度稀缺的领域,AlphaFold3也展现出了非凡的泛化能力。以CASP15的RNA预测任务为例,在几乎没有RNA训练数据的情况下,AlphaFold3在10个公开靶点上的平均表现超越了专门的RNA结构预测模型,这一成就无疑彰显了其强大的适应性和预测能力。
AlphaFold 3的突破之处在于其全面预测生命分子结构及相互作用的能力。其预测范围广泛,不仅覆盖了巨大的蛋白质、DNA、RNA分子以及离子和化学修饰组成,还包括了小分子配体药物等所有生命分子的三维结构。更为重要的是,AlphaFold 3还能预测这些分子之间的相互作用和组合方式,成为首个能够统一预测生命分子全貌的人工智能系统。
在预测精度方面,AlphaFold 3同样表现卓越。在关键的分子相互作用预测上,如蛋白质与配体、抗体结合等,其准确率比现有最佳方法高出50%以上,部分类型的相互作用预测准确度更是实现了翻倍。这一成就使AlphaFold 3成为首个在分子结构预测上超越传统物理方法的AI系统。
AlphaFold 3在预测类药物相互作用方面的准确性也达到了前所未有的高度。Isomorphic Labs正将AlphaFold 3与一套互补的内部AI模型相结合,致力于内部项目以及与制药合作伙伴的药物设计。这一结合无疑将加速药物研发过程,为医学领域带来革命性的变革。
在预测方式上,AlphaFold 3采用了全新的Evoformer深度学习架构,并通过类似图像生成的扩散模型进行整体计算。这种端到端的预测方式避免了将问题分解成子问题分步解决的繁琐过程,大大提高了预测效率和准确性。
要知道,AlphaFold3建立在AlphaFold2的基础上,但在架构和训练过程上有很大改进,也是其成功的关键:
遗传特征编码器(MSA module)被大幅简化,聚焦提取更关键的进化信息。
成对残基关系编码器(Pairformer)取代了原有的进化特征处理单元(Evoformer),增强了复杂相互作用模式的建模能力。
结构生成器从以氨基酸为中心,改为直接预测原子坐标,增加了处理通用分子结构的灵活性。
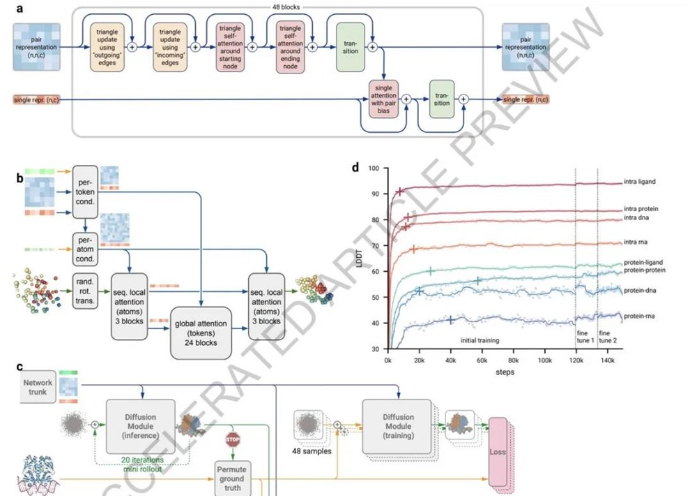
为了避免扩散方法在一些无结构区域产生幻觉,还引入了一种新的交叉蒸馏方法,通过AlphaFold-Multimer v2预测的结构数据来丰富训练数据。
AlphaFold 3的推出无疑为生物学研究和药物创新带来了革命性的影响。通过单一模型对整个生命分子王国进行高精度、整体性预测的能力,将使得生物学研究更加高效和深入。同时,AlphaFold 3在药物设计领域的应用也将加速新药研发过程,为医学领域带来更多的突破和进步。






 川公网安备 123456789号
川公网安备 123456789号